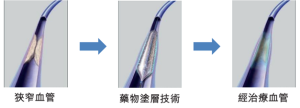
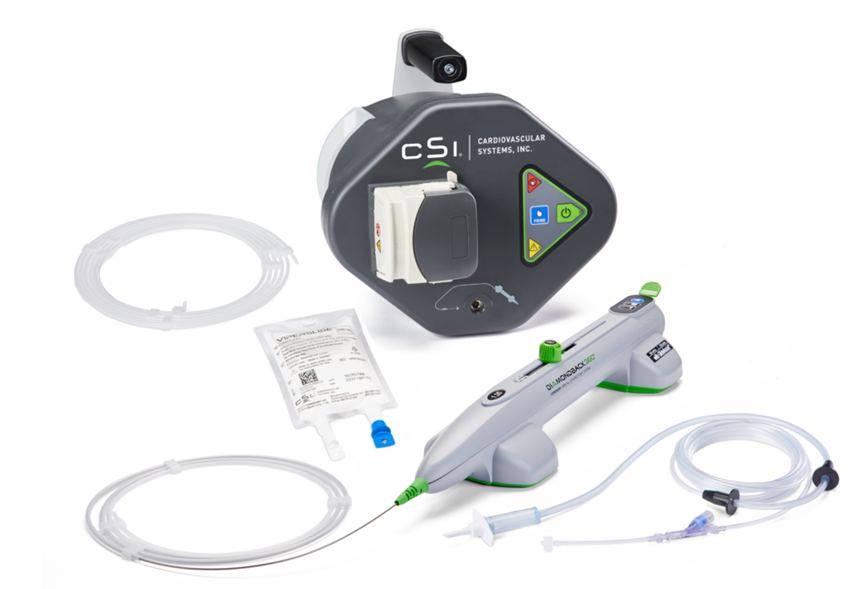
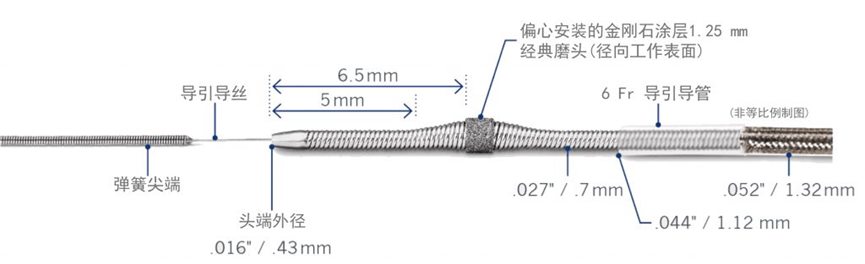
外周动脉疾病最常见的症状为间歇性跛行,休息后症状消失。中国外周动脉疾病患者由2014年的4,377万人增长到2018年的4,843万人,预计2023年患病人数将增长至5,596万人。目前针对外周动脉闭塞的两种主要非手术治疗方式是球囊成形术和置入外周动脉支架。
本文主要介绍药物球囊扩张导管、外周支架以及动脉血管减容产品。
一、外周动脉药物球囊扩张导管
全球首款药物涂层球囊(DCB)产品于2009年在欧洲上市。球囊扩张导管主要由球囊、导管和导丝组成。DCB目前已获国家药监局批准用于治疗冠状动脉疾病、下肢动脉疾病(LEAD)和透析患者动静脉通路增生。
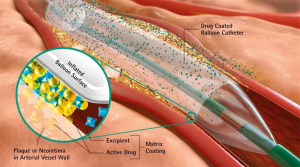
与经皮腔內血管成形术(PTA)球囊相比,DCB涂有的抗增殖药物,如紫杉醇或雷帕霉素,脂溶性紫杉醇常用于大多数商用DCB,原因是目前水溶性的雷帕霉素组织吸收率低,并且在组织中保留时间较短1。球囊膨胀时将药物释放至血管壁,阻止细胞分裂,限制再狭窄或阻止内皮细胞再生长。DCB的作用机理如下图所示:
再强大的医疗器械也离不开细小的精密部件。医疗器械展览会现场涵盖各类精密部件,包括液态硅胶部件、硅胶管件、橡胶模压件、球囊子宫支架、产后止血球囊、采血针、内瘘针、留置针、胰岛素针、齿科针、波形弹簧、无耳螺旋弹性挡圈、骨科手术器械,特种针头、消化道支架编织模具、疝气修补手术器械、头颅钻头……应有尽有。
DCB的主要核心区别在于使用何种药物以及如何将其附于球囊表面。一套理想的药物递送系统需要具备如下特点:
(i)于球囊达至靶病变前有效将药物固定在适当位置,因此药物不会容易被血流冲洗;
(ii)于球囊一经到达病变靶区时迅速将药物由球囊表面转移至血管内膜,从而缩短手术时间;
(iii)在靶病变中长期持续释放适当剂量药物,从而确保起有抑制内膜增生的长远疗效。
 外周血管用紫杉醇 DCB 产品的安全性相关技术审评关注点为微粒、药物释放、药物代谢和临床不良事件(死亡、截肢、靶病变的血运重建)发生率。
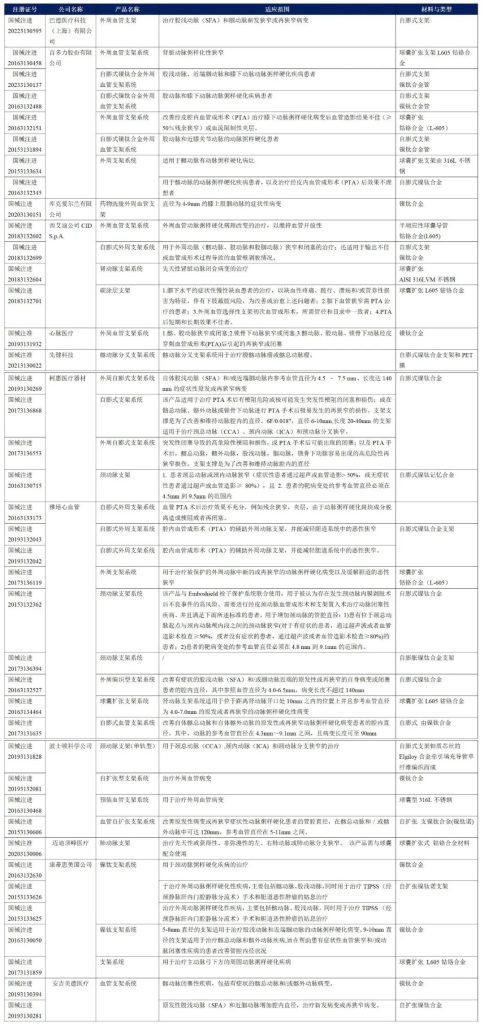
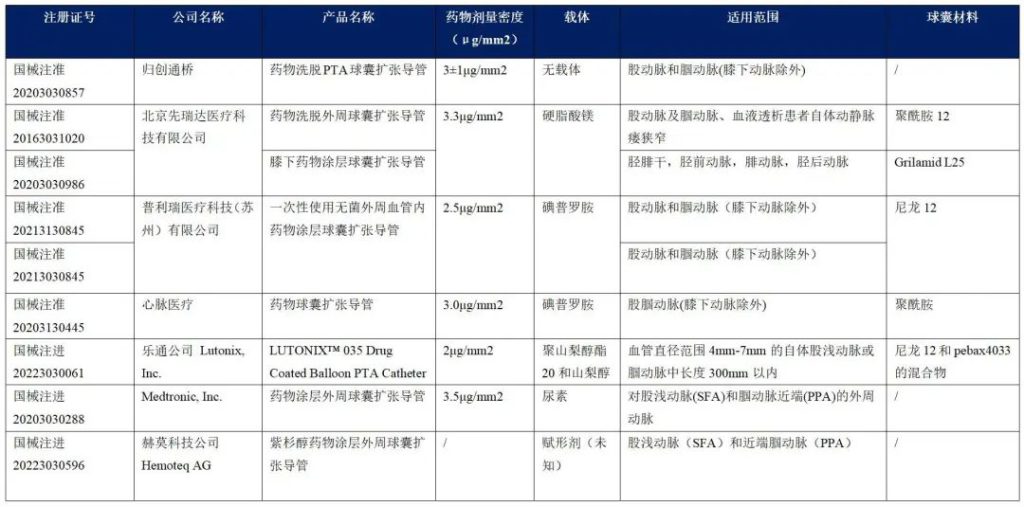
截止到2023年6月28日NMPA批准上市的DCB产品如下表所示(药物涂层均为紫杉醇)3:
外周血管用紫杉醇 DCB 产品的安全性相关技术审评关注点为微粒、药物释放、药物代谢和临床不良事件(死亡、截肢、靶病变的血运重建)发生率。
截止到2023年6月28日NMPA批准上市的DCB产品如下表所示(药物涂层均为紫杉醇)3:
 对于球囊扩张导管类产品,首先应符合强制性行业标准 YY0285.1 《血管内导管一次性使用无菌导管第1 部 分:通用要求》和YY0285.4 《血管内导管 一次性使用无菌导管 第4部分:球囊扩张导管》的相关要求。其次,国家药品监督管理局发布实施了《球囊扩张导管注册技术审查指导原则》。
由于 DCB 中含有紫杉醇涂层,还应对涂层的相关性能进行设计验证,建议对紫杉醇鉴别、涂层外观、紫杉醇含量和均匀性、杂质、紫杉醇体外释放、紫杉醇在球囊上的分布均匀性、微粒数量、微粒定性分析等项目进行深入的实验室研究。
DCB 脱落的微粒包括两种:一是产品自身产生微粒,即球囊表面的药物涂层在产品输送、扩张、回撤过程中脱落产生的微粒,主要包括药物和载体;另一种是生产过程中引入的不溶性微粒。
紫杉醇涂层 DCB 在血管内到达靶病变前以及球囊扩张过程中会因涂层脱落产生微粒,未进入血管壁的微粒可能会导致循环系统远端栓塞。FDA 已批准的紫杉醇 DCB(6 mm×80 mm)微粒测定结果如下表所示4。
对于球囊扩张导管类产品,首先应符合强制性行业标准 YY0285.1 《血管内导管一次性使用无菌导管第1 部 分:通用要求》和YY0285.4 《血管内导管 一次性使用无菌导管 第4部分:球囊扩张导管》的相关要求。其次,国家药品监督管理局发布实施了《球囊扩张导管注册技术审查指导原则》。
由于 DCB 中含有紫杉醇涂层,还应对涂层的相关性能进行设计验证,建议对紫杉醇鉴别、涂层外观、紫杉醇含量和均匀性、杂质、紫杉醇体外释放、紫杉醇在球囊上的分布均匀性、微粒数量、微粒定性分析等项目进行深入的实验室研究。
DCB 脱落的微粒包括两种:一是产品自身产生微粒,即球囊表面的药物涂层在产品输送、扩张、回撤过程中脱落产生的微粒,主要包括药物和载体;另一种是生产过程中引入的不溶性微粒。
紫杉醇涂层 DCB 在血管内到达靶病变前以及球囊扩张过程中会因涂层脱落产生微粒,未进入血管壁的微粒可能会导致循环系统远端栓塞。FDA 已批准的紫杉醇 DCB(6 mm×80 mm)微粒测定结果如下表所示4。
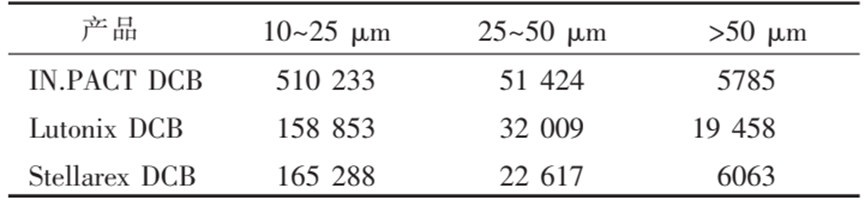 根据《中国药典》对静脉用注射剂中不溶性微粒大小及数量的要求,采用光阻法测定时,≥10 μm 的微粒不超过 6000 粒,≥25 μm 的微粒不超过 600 粒。虽然不同研究者采用的方法不同, 但测定结果均显示紫杉醇 DCB 产生的微粒数量不符合药典要求。
体外药物释放—体外药物释放研究在血管模型中进行推送、球囊扩张、球囊卸压、回撤,测定各步骤释放的药量以及残留药量,进而评估进入体内以及血管壁的药量,得出药物利用率。DCB 需要在球囊扩张时释放足量的药物且药物能进入血管壁,要求输送、回撤过程的药物损失以及球囊上残留的药物尽可能少。同时还需要研究未进入血管壁的药物去向。
动物实验—药物在体内的释放及代谢是需要额外关注的内容,是动物试验的评价重点。用动物试验评估进入血管壁的药量更具参考意义。药代动力学重点关注血液、靶血管以及远 端组织中的药物浓度变化情况。
临床评价—临床安全性评价指标一般为不良事件发生率,包括死亡、截肢、靶病变的血运重建。我国已上市产品公开审评报告显示,试验组与对照组在上市前临床试验截肢率差异没有统计学意义,但靶病变血运重建率 DCB 试验组明显低于对照组。
根据《中国药典》对静脉用注射剂中不溶性微粒大小及数量的要求,采用光阻法测定时,≥10 μm 的微粒不超过 6000 粒,≥25 μm 的微粒不超过 600 粒。虽然不同研究者采用的方法不同, 但测定结果均显示紫杉醇 DCB 产生的微粒数量不符合药典要求。
体外药物释放—体外药物释放研究在血管模型中进行推送、球囊扩张、球囊卸压、回撤,测定各步骤释放的药量以及残留药量,进而评估进入体内以及血管壁的药量,得出药物利用率。DCB 需要在球囊扩张时释放足量的药物且药物能进入血管壁,要求输送、回撤过程的药物损失以及球囊上残留的药物尽可能少。同时还需要研究未进入血管壁的药物去向。
动物实验—药物在体内的释放及代谢是需要额外关注的内容,是动物试验的评价重点。用动物试验评估进入血管壁的药量更具参考意义。药代动力学重点关注血液、靶血管以及远 端组织中的药物浓度变化情况。
临床评价—临床安全性评价指标一般为不良事件发生率,包括死亡、截肢、靶病变的血运重建。我国已上市产品公开审评报告显示,试验组与对照组在上市前临床试验截肢率差异没有统计学意义,但靶病变血运重建率 DCB 试验组明显低于对照组。
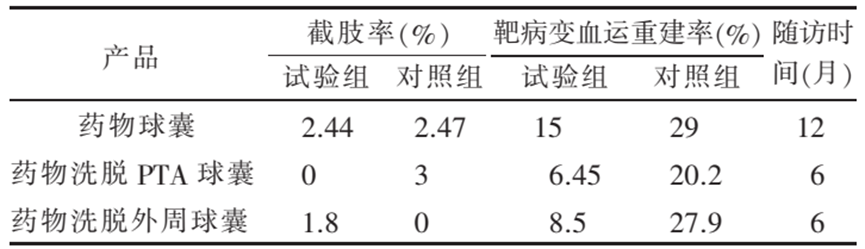 目前上市前的临床试验未能随访 2 年以上, 在远期安全性评价方面尚无充足的数据,留待上市后继续研究。
外周动脉支架分为球扩张支架和自扩张支架,球扩张支架主要应用于不会有明显变形的血管部位;而自扩张式支架是目前外周介入治疗中应用最多的支架,使用激光雕刻镍钛超弹合金管,材料的超弹性优异,在很小的鞘管内不会发生塑性变形。
由于支架在股浅动脉和腘动脉需要承受巨大的变形,因此自扩张支架在下肢动脉面临最大的问题是易发生疲劳断裂。针对股浅动脉,建议植入具有高耐疲劳性能的镍钛支架,而针对腘动脉,则不建议植入支架。
通过NMPA查询外周血管支架系统获批的厂家如下表所示:整体趋势来看,国产支架产品较少,以进口产品为主,另外现有上市产品更多是针对下肢动脉疾病,主要原因是下周疾病患者基数较大。国产厂家目前仅有心脉医疗有相关的下肢动脉支架产品。同时国外公司适用的适应症也相对更加丰富。
通过检测关键词“血管支架”“支架系统”“自膨式”“药物洗脱”“外周支架”“球囊扩张”,截止到2023年7月4日不完全统计,适用于外周动脉疾病的支架,不包含胸主动脉腹主动脉支架进口及国内公司共有39张注册证,其中国产3张注册证,心脉医疗、迈迪顶峰以及先健医疗各一张注册证。
减容技术可按减容成分的不同分为以去除血栓成分为主的技术(导管溶栓术、血栓抽吸术等)和以去除硬化斑块成分为主的技术(斑块旋切术、激光消融术等)6。导管溶栓术、血栓抽吸术等在外周静脉疾病中具体展开。
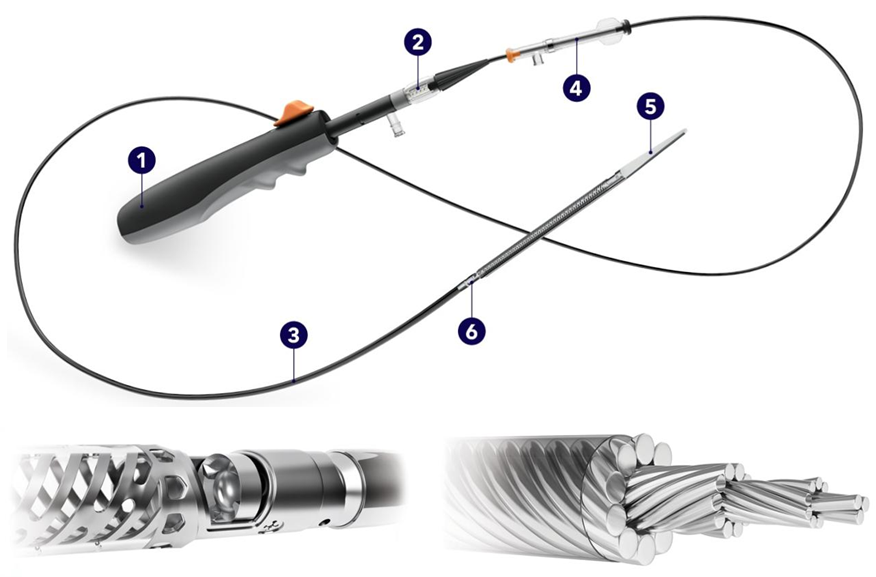
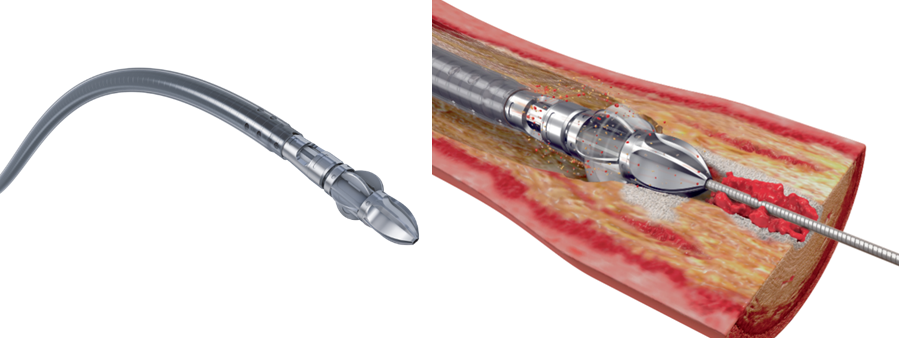
斑块旋切术是指在血管腔内,用高速旋磨钻头切除血管壁斑块组织或将斑块研磨乳化成微小颗粒,以达到消除或减轻管腔狭窄、拓宽管腔的微创技术。斑块旋切术的优势有以下几方面7:
定向斑块旋切系统是最早进入中国市场的斑块旋切设备,SilverHawk 是其第一代产品。优势主要体现在体内不留存异物和可重复操作。SilverHawk 斑块旋切术的远期通畅率并不能令人满意,特别是对于长段完全闭塞性病变的患者。
HAWK 系统的新一代产品 TurboHawk 进入中国市场, 其在刀头设计、驱动方式、转速等方面做了改进,使切割效率提高,对严重钙化病变同样有效。
HawkOne:是最新型号,拥有适合所有类型钙化斑的刀片以及两种不同长度锥形收集导管型号,有导致远端血管栓塞的风险,可在栓塞保护装置存在的前提下使用,该设备的血管鞘管兼容性为6 -7 F。
目前上市前的临床试验未能随访 2 年以上, 在远期安全性评价方面尚无充足的数据,留待上市后继续研究。
外周动脉支架分为球扩张支架和自扩张支架,球扩张支架主要应用于不会有明显变形的血管部位;而自扩张式支架是目前外周介入治疗中应用最多的支架,使用激光雕刻镍钛超弹合金管,材料的超弹性优异,在很小的鞘管内不会发生塑性变形。
由于支架在股浅动脉和腘动脉需要承受巨大的变形,因此自扩张支架在下肢动脉面临最大的问题是易发生疲劳断裂。针对股浅动脉,建议植入具有高耐疲劳性能的镍钛支架,而针对腘动脉,则不建议植入支架。
通过NMPA查询外周血管支架系统获批的厂家如下表所示:整体趋势来看,国产支架产品较少,以进口产品为主,另外现有上市产品更多是针对下肢动脉疾病,主要原因是下周疾病患者基数较大。国产厂家目前仅有心脉医疗有相关的下肢动脉支架产品。同时国外公司适用的适应症也相对更加丰富。
通过检测关键词“血管支架”“支架系统”“自膨式”“药物洗脱”“外周支架”“球囊扩张”,截止到2023年7月4日不完全统计,适用于外周动脉疾病的支架,不包含胸主动脉腹主动脉支架进口及国内公司共有39张注册证,其中国产3张注册证,心脉医疗、迈迪顶峰以及先健医疗各一张注册证。
减容技术可按减容成分的不同分为以去除血栓成分为主的技术(导管溶栓术、血栓抽吸术等)和以去除硬化斑块成分为主的技术(斑块旋切术、激光消融术等)6。导管溶栓术、血栓抽吸术等在外周静脉疾病中具体展开。
斑块旋切术是指在血管腔内,用高速旋磨钻头切除血管壁斑块组织或将斑块研磨乳化成微小颗粒,以达到消除或减轻管腔狭窄、拓宽管腔的微创技术。斑块旋切术的优势有以下几方面7:
定向斑块旋切系统是最早进入中国市场的斑块旋切设备,SilverHawk 是其第一代产品。优势主要体现在体内不留存异物和可重复操作。SilverHawk 斑块旋切术的远期通畅率并不能令人满意,特别是对于长段完全闭塞性病变的患者。
HAWK 系统的新一代产品 TurboHawk 进入中国市场, 其在刀头设计、驱动方式、转速等方面做了改进,使切割效率提高,对严重钙化病变同样有效。
HawkOne:是最新型号,拥有适合所有类型钙化斑的刀片以及两种不同长度锥形收集导管型号,有导致远端血管栓塞的风险,可在栓塞保护装置存在的前提下使用,该设备的血管鞘管兼容性为6 -7 F。