
摘要:随着医学检测和仪器仪表工程技术的不断提高,体外诊断仪器设备的技术、设计、测试和开发方法正快速地发展。体外诊断仪器也逐渐发展成为一类典型的高端医疗设备。体外诊断仪器的设计涉及到多种多样的医学诊断方法,生化、物理等相关技术及其应用开发过程还涉及到复杂的系统工程。该综述对二者进行了系统地总结与概述了体外诊断仪器的设计、测试和研发方法以及其近年来的发展,重点总结了相关技术以及研发程序的核心层面,并对体外诊断仪器市场的发展趋势进行了分析。
关键词:体外诊断仪器;设计;测试与开发方法;系统工程;市场趋势;
【引言】
体外诊断 (IVD) 仪器是通过检测人体样本(各种体液、细胞、组织样本等),在人体外用于获取临床诊断信息,进而确定疾病或发动机机体功能的产品。体外诊断仪器在医学领域被称为“医生的眼睛”,是现代检验医学的重要组成部分。IVD仪器的临床应用贯穿于疾病诊疗的全过程,包括疾病预防、初步诊断、治疗方案选择和疗效评价,为医生提供大量有用的临床诊断信息,越来越成为人类疾病诊断和治疗的重要组成部分。
体外诊断仪器作为一类高度专业化的仪器,需要在医学检验科学和体外诊断方法学的基础上进行设计和开发。随着体外诊断方法学、检测相关技术、仪器工程技术等多个领域的发展,体外诊断设备设计越来越精细,逐渐进入高端医疗设备研发的先进水平。体外诊断可分为生化诊断、免疫诊断、分子诊断、微生物诊断、血液诊断、(患者)床旁检测 (POCT) 等。涉及的相关技术包括电化学技术、波谱技术、色谱技术、质谱、电泳、流式细胞术、标记免疫学、分子生物学、生物传感技术等。体外诊断仪器种类繁多,研发过程一般包括产品项目设计、产品原型开发、产品定型器开发、产品验收等阶段,每个阶段都是基于一定的规则。
该2024医疗器械展会Medtec综述系统地组织和总结了体外诊断器械的设计、开发、测试方法和最新进展,重点介绍了研发过程的相关技术与核心层面。第二节首先介绍体外诊断方法和体外诊断器械的发展过程,然后对体外诊断器械的相关技术和应用进行总结分析,从应用角度对体外诊断器械进行分类并举例说明,最后重点介绍了体外诊断器械的开发过程及其关键方面。第三节分析了体外诊断器械的市场发展趋势,介绍了未来发展的重点方向。第四节从体外诊断器械技术发展方向进行了初步讨论。体外诊断仪器种类繁多,涉及的领域和知识范围巨大,技术的设计、测试和发展都在不断发展,不可能对体外诊断器械研发的整个范围提供完整、详细的总结,故该综述只是某些角度的初步汇编。
2.体外诊断方法与仪器的开发
体外诊断仪器的设计、测试和开发基于医学检测和体外诊断方法。体外诊断设备作为集检验与工程于一体的系统仪器,种类繁多,型号繁多,涉及电化学、光谱、色谱、质谱、电泳、流式细胞、标记免疫学、分子生物学等学科,可支持多种检验项目。同时,类似于其他类型的综合设备的研发过程,体外诊断设备的研发需要经历产品项目设计、原型研发、产品型和产品验收等关键阶段,此外,还包括临床试验以及医疗行业特别要求的法律和监管程序。本节将提供体外诊断方法学进展、相关技术和应用、体外诊断器械分类和研发过程的系统概述和总结。
2.1 体外诊断方法学的发展
同生物化学、免疫学、分子生物学等领域的发展一道,体外诊断产业的发展可以分为三个阶段:
第一阶段:20世纪前,显微镜的发明诞生了基于微生物显微镜检查的传统手段。
第二阶段:20世纪初,现代医学的发展以及酶催化反应和抗原抗体反应的发现为生化和免疫学诊断奠定了基础,体外诊断逐渐兴起。
第三阶段:20世纪50年代后,DNA双螺旋结构、单克隆抗体技术和巨大分子标记技术等技术的运用推动了分子诊断以及整个体外诊断行业的跨越式发展。
第三阶段是体外诊断行业核心技术的主要发展阶段。从1950年到1970年,体外诊断产业进入发展阶段。从1970年到1980年,行业进入快速发展期。自1980年以来,体外诊断新技术逐渐兴起。演变图如图1所示。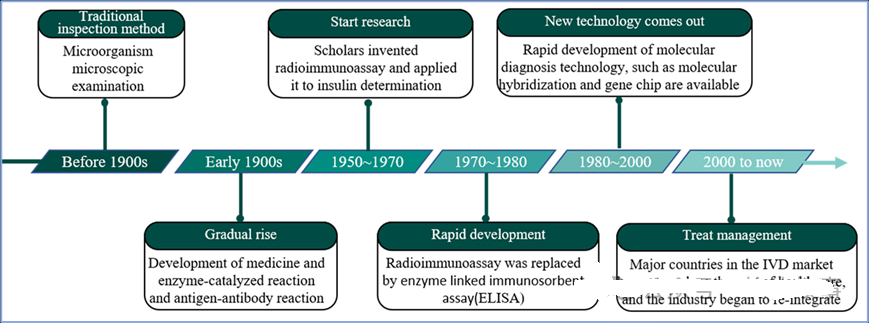
图1 图解体外诊断产业的历史发展
根据诊断原理和方法的不同,体外诊断方法学可分为生化诊断、免疫诊断、分子诊断、
微生物诊断、血液诊断、POCT等。表1整理了目前体外诊断的主要方法以及相关原理、技术与应用领域。
表1.体外诊断主要方法学的分类
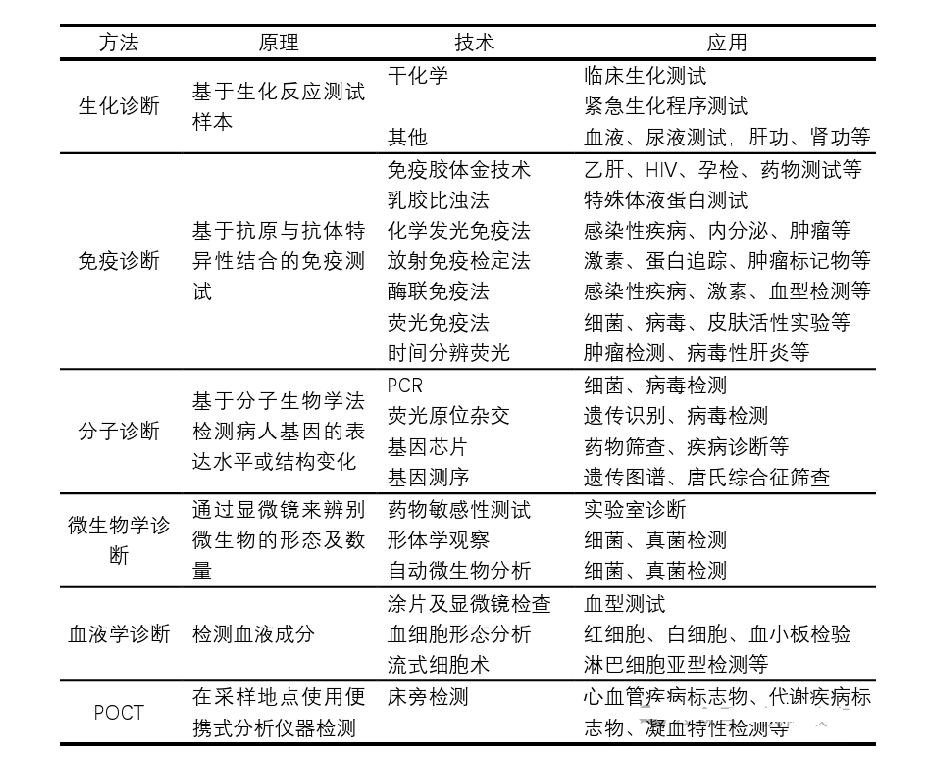
2.2 体外诊断器械相关技术及其应用
虽然临床应用的体外诊断仪器种类繁多,但这些仪器的设计和开发始终基于相关技术的产生和发展。体外诊断设备是以临床和实验室检验方法学为基础,结合自动化技术、光学技术、电子信息技术、生物传感技术、计算机技术等,并逐渐发展成为系统、工程化的现代仪器和设备,以满足临床试验和医疗服务的需求。
2.2.1 电化学分析技术:
电化学分析是将待测物质的溶液形成化学电池,通过测量电池的电位、电流、功率和电阻等变量,将待测物质的浓度转换成电参数,从而进行检测的一种分析技术。电化学分析技术可分为电位分析、电导率分析、电解分析、电容分析、Volt-Anne分析和电化学生物传感单元技术。
临床生化检测中用于电解质分析、血气和酸碱度分析的仪器大多是基于电化学分析技术。电化学发光免疫分析 (ECLIA) 是将电化学反应引起的化学发光过程与免疫反应过程相结合的新技术。
ECLIA 既具有发光检测的高灵敏度,又具有免疫分析的高特异性。基于 ECLIA 技术的电化学自动化免疫分析仪已广泛应用于临床免疫学检测,包括肿瘤标志物、激素、酶、抗原或抗体、维生素、细胞因子和各种代谢物的测定。
2.2.2 光谱分析技术
光与物质的相互作用是自然界中普遍存在的物理现象。借助这两者之间发生相互作用时产生的吸收、发射或散射光谱的不同波长和强度来表征和定量检查某一物质的技术称为光谱分析技术。依据光谱的产生方式,可将光谱分析技术分为三大类:吸收光谱分析、发射光谱分析和散射光谱分析。采用光谱分析技术的体外诊断仪器,结构相对简单,操作简便,方法相对灵敏,因而广泛应用于临床检验。
根据物质辐射能量的分子或原子对选择性吸收获得的分子或原子光谱为吸收光谱。吸收光谱分析包括紫外-可见光分光光度法、红外光谱法和原子吸收分光光度法。紫外-可见光分光光度法主要用于物质的定量检查,如血清无机磷。原子吸收分光光度法主要用于金属元素的分析测定,如测定血液中锌、镁、铜的含量。
发射光谱是物质的分子、原子或离子接受外界能量,从基态跃迁到高能态,然后从高能态返回到基态时出现的光谱。发射光谱分析技术涉及使用发射光谱通过定量检查对物质进行表征。荧光分光光度法更常用于临床检测。例如,可使用荧光分光光度法测定维生素含量。
光子作用于非均匀电介质时,会产生光散射现象;而通过测量漫射光的强度得到待测物质含量的方法便是散射光谱分析法。当光源的光通过待测样品时,样品中的抗原与其特异性抗体形成抗原抗体复合物,使溶质颗粒增多,光散射增强,漫射光的强度与复合物的含量成正比。因此,抗原含量可以从散射光强度的变化来测量。基于散射比浊法的全自动散射浊度分析仪被广泛应用于临床,其主要用于测定体内的蛋白质物质,如血清免疫球蛋白、C反应蛋白和尿液中的微量蛋白等。
2024医疗器械展会Medtec将同期举办ADTE展会,汇集国内外知名体外诊断相关企业,丰富的展品等你现场来看!现在注册参观预登记还可免费参与展会现场同期会议,论坛议题涵盖法规政策、质量管理、产品设计、塑模成型、包装灭菌等。提前预登记还可享受好礼>>>
2.2.3 色谱分析技术
色谱法是一类分离和分析技术的总称,主要用于复杂多组分混合物的分离和分析。色谱法使用组分不混溶的混合物两相之间的差异分配因子,同时分离物质的组分,然后进行表征或定量测定。
色谱分析法种类繁多;根据流动相性质可分为液相色谱法和气相色谱法;根据分离原理可分为吸附色谱法、分布色谱法、离子交换色谱法等;柱层析和平面层析根据固定相状态。临床检验中常用的色谱技术也成为柱层析技术。高效液相色谱法 (HPLC) 是在经典色谱方法的基础上,通过改变高压输送的移动相,用小粒径填料填充色谱柱,使柱效显著地提高,并通过连接高灵敏度的检测装置,提高了对出水的连续检测效率。HPLC 适用于具有生理活性的大分子物质的分离纯化,如蛋白质、酶、激素、单氨基酸、核酸等。
2.2.4 质谱分析技术
质谱 (MS) 是根据质荷比的数量级来排列绘制的带电原子、分子或分子碎片图。质谱仪是能将物质的粒子解离成离子的一类仪器,通过适当的电场或磁场,根据其空间位置、时间顺序或轨道稳定性将其分离,以达到质荷比,并在检查强度后对物质进行分析。
虽然质谱能够进行定性分析,但不能分析混合物,而色谱可有效分离混合物;两者结合可同时分离和鉴别,从而产生质谱耦合技术。目前的质谱仪主要有以下耦合方式:气相色谱-质谱耦合技术、液相色谱-质谱(LC-MS) 耦合技术、串联质谱技术等。质谱技术因其分析灵敏度高、样品消耗低、分析速度快和能够同时集成分离鉴定等特点,从而被广泛应用于临床医学。
当出现骨代谢异常、糖尿病、心血管疾病、肿瘤等疾病时,不同群体的维生素D减少或缺乏。LC-MS技术具有高度特异性,能够同时测定25-(OH)维生素D2和25-(OH)维生素D3;被认为是检测25-(OH)维生素D的金标准,在临床应用中越来越普遍。此外,质谱分析技术还广泛应用于一些药物和兴奋剂的检测。
2.2.5 电泳分析技术
电泳是指分散在介质中的带电粒子在电场作用下向电场的正极移动,正电荷粒子向电场的负极移动的现象。利用电泳现象分离物质的技术称为电泳分析技术。电泳分析技术主要用于蛋白质和核酸的分离、鉴定和定量检查。电泳技术可分为流动界面电泳、区带电泳和稳态电泳;根据固相支持介质又可将其分为两类:一类是滤纸、乙酰纤维素膜电泳,另一类是琼脂糖凝胶、聚丙烯酰胺凝胶电泳。
而等电聚焦电泳仪、双向电泳系统、垂直电泳系统和全自动电泳分析仪的开发和应用,使得电泳带的分离越来越清晰,操作更加简便。常用的水平电泳仪主要用于血清蛋白、血红蛋白、同工酶等的分析。
2.2.6 流式细胞分析技术
流式细胞术(FCM)结合了激光、流体力学、计算机和电子测量技术,实现了移动过程中快速而准确的细胞测量。FCM可以测量细胞大小、形状、核质比、色素含量、胞浆颗粒等。当荧光染料进入细胞后,其还可以测量细胞核内的核酸含量、染色质结构、细胞表面抗原或糖分子、细胞骨架等。FCM具有灵敏度高、分辨率高、分选纯度高、可重现性高和多参数信息综合分析等优点,提供快速、准确的细胞及其相关成分的定量检查和分选。
在临床免疫测定中,FCM主要通过检测细胞表面的分化抗原进行淋巴细胞亚群、造血干细胞、抗原呈递细胞等来分析和测量细胞表面抗原。
2.2.7 标记免疫分析技术
标记免疫分析技术是各种临床免疫学检测的基本技术,一般是指用不同的物质标记抗原或抗体,使其具有示踪功能且具有抗原抗体的特异性反应,以达到检测临床标本中待测物质的目的。目前临床免疫学检测的主要标记免疫学技术包括荧光免疫学技术、放射免疫技术、酶免疫学技术、化学发光免疫学技术和电化学发光免疫学技术等。用作示踪剂的主要标记物质是荧光素、放射性核素、酶蛋白、化学发光剂和电化学发光剂。
2.2.8 分子生物学分析技术
分子生物学分析技术已成为临床检验中检测各种病原微生物核酸、检测遗传性疾病致病基因以及检测一些疾病相关基因和代谢物基因的重要技术之一。
临床检测中最常用的分子生物学技术是聚合酶链反应 (PCR),其是一种体外扩增基因的技术。目前临床检验应用最多的是荧光定量PCR技术,其能够对靶分子进行定量检查,如乙肝、丙肝病毒核酸的定量测定,而这正是疾病诊断和药物疗效观察的重要依据。
2.3 体外诊断仪器的分类
体外诊断产品主要由诊断设备和诊断试剂组成。其中,体外诊断仪器属于临床检验分析仪器范畴。体外诊断器械种类繁多,几乎涵盖了所有的医学检测项目。表2总结了常见体外诊断仪器的当前分类,以及一些代表性产品。
表2.体外诊断仪器分类

2.4 体外诊断仪器的系统性设计、测试与程序开发
与其他种类综合仪器的研发过程类似,体外诊断器械的设计开发也是一个系统的项目。产品开发没有一定的规律,需要根据具体的体外诊断设备和研发生产团队的特点来规划。但从工程角度来看,体外诊断器械的设计、测试和开发过程一般要经过产品项目设计、产品原型开发、产品定型和产品验收等重要阶段。
此外,由于医疗行业的特殊特点,体外诊断器械在投产前往往要经过临床试验和评价,以及相关的法律法规验证阶段。
根据相关的政策法规、行业标准和法规文件,项目经理应完成产品的整体方案设计。这一过程一般包括产品设计要求、试验方法、试验原理、产品结构组成、产品功能指标、产品性能指标、产品主要工作流程、模块化结构设计、产品成本预算等。如果产品必须进入其他国家或地区市场,则需要满足当地法规的要求。然后,相关人员对总体方案进行审核,提出修改意见或建议,并持续改进。
根据各模块的结构组成和尺寸,广泛确定产品形状的结构、规格和设计风格。良好的外形设计可以使产品在市场上占主导地位,增强产品的综合竞争力,降低生产成本,增加对客户的青睐。因此,形式评价是研发过程中不可或缺的一部分。
为使软件开发人员、用户和测试人员清楚地了解软件的功能,软件描述应尽可能详细,包括接口样式、用户需求、相关产品需求的描述,软件与系统总接口、运行环境、系统功能、安全要求等的关系。其中,软件体系结构设计主要描述软件组件的类型和系统运行的重要功能模块;软件描述文档需根据软件和网络安全相关的法规、标准和技术管理原则进行编写。硬件系统设计与评估
首先是进行专利分析,针对侵权可能性、衍生专利、技术成果可专利性等问题,基于每个模块对设计结果进行专利纠纷。接下来便是进行硬件系统技术质量标准指导手册的开发,包括详细描述硬件系统的组成、系统开发的要求、主要技术指标、硬件的需求分析、各模块的布局结构、与计算机的接口设计等。随后,相关人员将对技术质量标准说明书进行审核,提出修改意见或建议,并不断改进,审核通过后进入下一流程。
此模块需制定以下内容:核心模块技术质量标准指导手册,详细描述了模块设计的结构、以及所需的软件支持、待实现的功能、性能指标和形成核心模块设计方案所需的操作环境。随后,相关人员对模块项目设计进行审核,提出意见或建议修改,然后不断改进,待审核通过后再进行下一步流程。
首先,确定产品的基本模块化结构和每个模块的近似尺寸,以便实现产品的功能和性能。接下来,确定系统运行所依赖的软件,包括执行系统、接口软件和每个模块的近似大小。然后,建立了机械图纸、电路板和工具(如使用的软件及其版本号)的详细设计和确认。
硬件系统的详细设计需要完成如下。(1) 电气结构设计:确定所选控制组件的数量及其参数,以及模块如何装配在一起。(2) 物理结构设计:根据电气组件的大小,确定如何匹配机械零部件和安装。(3) 功能结构设计:确定参数选择。(4) 器械选择:根据组件手册中的参数,确定器械型号;或根据主流型号的设计,在达到相同功能的前提下,选择销量最大,组件供应充足。(5) 绘制印刷电路板:根据电路功能需要,设计示意图后再设计印刷电路板图。(6) 硬件系统的详细设计评审:相关人员应评审硬件系统详细设计,做出变更或建议,然后继续改进,评审进入下一过程。
软件系统的详细设计需要规定软件系统的主要业务需求、输入、输出、主要功能、性能指标和运行环境;软件开发使用的语言、工具和方法以及名称、完整版本、上述配套及应用软件需确定供应商。同时需要明确研发人员数量、开发时间、工作量和代码总行数,明确软件安全性级别,并详细说明确定理由。
软件生存周期分为需求分析、设计、编码、测试和维护五个阶段。器械系统的详细设计需要完成以下要点:(1)系统硬件拓扑结构:根据软件设计规格提供物理拓扑结构示意图,描述软件或组件模块、多用途计算机、医疗器械硬件之间的物理连接关系;(2) 系统结构图:利用结构图表示组件模块之间、组件模块与外设接口之间的关系,并依据系统结构图描述组件模块的功能、模块关系和外设接口;(3) 用户界面关系图:描述用户界面之间的关系,以用户界面关系图为基础,描述软件系统的功能和模块关系,以列出系统内各模块关系的图的形式;(4) 核心算法:描述核心算法中使用的计算公式和具体的计算步骤;(5) 程序逻辑:以过程流程图的形式,显示实现程序的逻辑流程;(6)运行环境:明确软件运行所需的硬件配置、软件环境和网络条件,包括硬件配置(包括处理器、内存和外围设备)、软件环境(包括系统软件、支持软件和安全软件)、网络条件(包括网络体系结构、网络类型(WAN、LAN、个人域网络)和带宽);(7)接口:描述与本程序相关的上层模块和下层模块之间的接口关系;(8)禁忌症:使用独立软件描述软件禁忌症或服务限制,软件组件描述医疗器械产品禁忌症或服务限制,进口医疗器械软件描述原产国。
设计工程是以物理形式表达设计计划的活动过程,包括计划和愿景。相关过程如下:
(1) 电气和光学模块设计:印刷线路板由电气原理图制成,电气原理图主要是根据各部件的电气性能进行合理的构造,通过该图可以准确反映印刷线路板的重要功能,以及各部件之间的关系。在完成电原理图设计后,再通过绘图软件对所选的单个部件进行打包,生成并实现具有相同部件外观和尺寸的网格。然后根据印刷线路板的尺寸放置单个组件;放置组件时,必须确保单个组件的导线不会交叉。在进行接线图设计的同时,先按电气原理图绘制接线楼层平面图;再按楼层平面图确定电气元器件的摆放位置,按设计图将电路板等元器件装配成模块。(2) 模块验证:设计工程师根据各模块在此阶段所能达到的功能和性能指标,制定模块确认计划;测试工程师根据确认计划进行确认,确认后出具确认报告。(3)电光模块设计评审:相关人员对电气和光学模块设计进行审核,提出修改意见或建议,然后不断改进,审核通过后进入下一步流程。(4) 机械、液压回路模块设计:首先根据设计确定部件,然后根据图纸加工或采购部件,并根据设计图纸组装成模块。(5) 模块验证:设计工程师根据各模块在此阶段所能达到的功能和性能指标,制定模块确认方案;测试工程师根据确认方案进行确认,确认后出具确认报告。(6)机械、液态电路模块设计评审:相关人员对机械、液态电路模块设计进行评审,提出修改意见或建议,然后不断改进,评审通过后进入下一步流程。
此过程旨在对整机进行装配接头和功能验证,包括如下步骤:
(1) 整个仪器组装:根据装配好的电气模块、光学模块、机械模块、液压模块,按图纸要求装入整机。(2) 开机前进行初始调整:通电前,根据图纸要求再次检查每个模块的相对位置,以避免通电后的碰撞和干扰。如检查内部组件布线是否正确,布线是否合理,紧固件安装是否牢固,运动部件旋转是否灵活等。(3)整机功能及性能验证:设计工程师根据产品在此阶段所能达到的功能和性能指标,制定整机初步验证计划,测试工程师根据初步验证计划进行验证,验证后出具验证报告。(4)电气安全验证:按照法规和国家标准的要求,对整机电气安全进行了验证。(5)环境适应能力验证:验证产品是否符合设计输入的环境要求,包括气候环境基线和机械环境基线。(6) 电磁兼容性 (EMC) 验证:根据法规和国家标准的要求,对整机电磁兼容进行了验证。(7)整机审核:相关人员对整机这一阶段要达到的安全性、有效性进行审核,提出修改意见或建议,然后不断改进,审核通过后进入下一步流程。
根据最终的设计结构对模具进行工程化改进。进行包装和标签设计以及包装容器和配件箱设计,并完善模块工艺文件。测试工程师根据仪器各模块的功能和性能准备测试用例,将软件测试行为转化为可管理的模式,同时量化测试工作。并准备关键组件列表,随后测试工程师根据原材料实施测试。
根据生成的物料清单和进度计划,采购部采购少量原材料。设计工程师根据各模块实现的功能和性能指标,对模块验证方案进行了改进。测试工程师根据制定的验证方案实施验证并做好相关记录。根据专家在模块审评过程中提出的意见或建议而完善模块并更新技术文件。
该过程包含制定整个仪器的初检、调试和老化标准。根据整机初检和整机老化运行过程中积累的经验和设计要求,制定整机初检和整机老化标准,从而指导生产。设计工程师根据产品装配情况,对关键主库进行检查,设计工装、检验所需的各关键主库,并遵循验收准则和使用说明书;如涉及软件,应统一编码存档。
此过程旨在使所开发医疗器械产品的整体功能和性能得到确认,包含如下步骤:
(1) 制定整机验证方案:根据整机功能和性能指标,设计工程师应完善整机验证方案,其中包括整机功能验证方案、整机性能验证方案、整机可靠性验证程序和整机类型验证程序。(2) 验证的实施:根据制定的验证方案,测试工程师应实施验证并做好相关记录。(3) 整机初检:检查整机安装的密封性,以及各独立部件和模块的相对位置。(4) 整机老化:产品组装调试完成后,整机将按照工艺文件规定的要求连续通电一段时间(视产品和时间而定),其目的是发现和消除电子元件通过老化而出现的早期故障,以及提高电子设备的工作可靠性和使用限度,同时稳定整机参数,保证调试质量。通常情况下,整机根据上电老化的以下方面进行考虑:温度、循环周期、累积时间、测试次数、测试空白时间等。(5) 整机调试:组装成整机的合格模块调试后,模块之间的合作不能全部处于最佳状态,满足整机技术指标;由此可见,需要将模块的相对位置和公差间隙调整到整机图纸要求的尺寸,使与各部件相关的工作处于最佳状态。(6) 机器性能检验:为验证仪器能否达到行业标准或产品技术要求的性能指标,并判断软件系统是否存在性能瓶颈进而优化软件,机器性能的检验是最关键的环节之一。项目检验应符合行业标准或产品技术要求的性能指标项目。(7) 软件测试:可以根据需要编写不同的测试软件工具,然后用于分析和评价测试程序可能存在的问题。
在完成医疗器械产品设计开发后,将对产品进行最终验收,并根据需要开展临床评价等工作。此过程包含如下步骤:
(1) 制定整机验证方案:对变更后的设计结构补充整机验证方案。(2) 验证的实施:根据制定的验证方案,测试工程师实施验证并做好相关记录。(3)临床适用性评价:医疗器械产品为临床应用产品,应在产品上市前对设计是否符合临床要求进行分析评价。分析中应包括临床评价期间收集的临床性能和安全性数据(包括有利和不利数据)。临床评价的深度和广度、所需数据类型和数据量应与产品的设计特征、尖端技术、适用范围和风险程度以及非临床研究的水平和程度相适应。临床评价应对产品的适用范围(如适用人群、使用部位、与人体接触方式、适应症、疾病的程度和阶段、使用要求、使用环境等)、使用方法、禁忌症、注意事项、警告等临床使用信息进行确认。
3. 体外诊断仪器的市场趋势
近些年来体外诊断的市场保持快速地增长。随着生活水平的不断提高,人们对健康的需求也与日俱增,体外诊断作为疾病诊断的重要手段也获得了飞速发展。近年来,许多国家大力推行医疗体制,废除药品耗材,出台控医保费、控消费比、控药比等一系列医院改革政策。医院作为一种经济体制,一直致力于医疗服务和诊断部门,以弥补其从药品和耗材上的收入损失,医疗服务和体外诊断将在这一方面和其他方面快速发展。预计体外诊断行业未来的三个重点方向如下:
免疫诊断是体外诊断市场中最热门的细分领域,约占40%的市场份额。随着技术的不断发展和进步,低端免疫诊断领域取得了较好的效果,但高端免疫诊断领域仍被几家巨头公司垄断,其中最具代表性的还是化学发光领域。目前,化学发光法已取代酶联免疫分析成为主流免疫诊断方法,其市场规模已达到免疫诊断市场总量的70%以上,基本被龙头公司垄断。未来,随着关键核心技术的突破和先进技术的引进,再加上鼓励创新的政策扶持,化学发光领域将取得重要突破,有望逐步实现高端免疫诊断领域的跨越式发展。
分子诊断法尚处于起步阶段,市场集中度低,规模小;但其增速较高,以超过25%的增速领先于体外诊断行业。分子诊断法作为生命科学领域最尖端的技术,目前已广泛应用于产前筛查、传染病、肿瘤等领域。分子诊断技术的发展时间相对较短,相关企业的技术水平差距相对较小,特别是在基因测序领域,涌现出了很多优秀和创新的企业。得益于精准医疗的发展趋势和分子诊断技术的不断升级,未来分子诊断将继续快速增长,而走在分子诊断前列的基因测序也将成为优质企业的主战场。
POCT具有不占据大空间、使用方便、高效且高精度、价格普遍低廉等诸多优点。POCT 通过确定病因和预后、提高治疗有效性和降低医疗费用,对疾病预防具有重要意义,可满足各级各类医疗机构的临床检验需求。尤其是在大力推进分级治疗和第三方检测的时候,低成本、高效率的POCT产品对基层医疗卫生机构和第三方检测机构更具吸引力。目前POCT市场整体规模不大,但发展较快;随着分级治疗政策的实施,POCT市场将快速发展,具有政策和成本优势的企业首次布局也将迎来进一步发展。
企业通过在产业链上占据合理位置,便可以有效提升竞争力。体外诊断产业主要由上游(电子元件、诊断酶、抗原、抗体等原料)、中游(诊断设备、诊断试剂)和下游(医院检验部门、医学检验中心、独立实验室、防疫站等)组成。上游原料市场、中游高端诊断市场、下游大医院市场以龙头企业为主;上游原料尤其被大企业垄断,这往往给其他企业带来困难,使其只能参与中低端市场的激烈竞争;即使在某一部分取得进展,也不能很好地转化为整体优势。
近些年来,这种情况逐渐开始改善;随着创新和进口替代政策的不断出台,创新企业加强了产业链布局和研发投入,在上中下游取得了良好进展。因此,专业化、规模化将成为企业突破性发展的最佳选择。
【讨论】
医学诊断科学发展最突出的标志是医学检验自动化代替传统的人工操作;人工分析测定精密度低、速度慢、难以标准化等缺点。其中尤以体外诊断仪器的设计开发和临床应用最为重要,对临床检验技术和现代医学的发展具有重要意义。临床常用自动化体外诊断仪器的技术原理大多基于传统的实验技术,如电化学技术、光谱技术、色谱技术、质谱、电泳、流式细胞术、标记免疫学、分子生物学、生物传感等。
体外诊断设备的发展过程体现了半自动化、自动化、一体化、小型化、高通量、智能化的特点,降低了检测成本,全面提高了分析测量的精密度和准确度,满足不同临床和患者情况的需求。体外诊断仪器可用于普通血液学分析、尿液分析、生化分析、免疫学分析、细胞免疫功能分析、血型鉴定、微生物培养鉴定、分子生物学检测等。几乎覆盖了临床检验实验室的所有专业和大部分检验项目,成为现代医学检验的重要工具。
体外诊断器械种类繁多,研发过程无法用一套固定的规范来定义。然而,通过整合医学试验方法学和工程学等理论和技术概念,有一套可参考的体外诊断器械的设计、试验和开发过程供参考。一般来说,体外诊断器械的设计和开发要经过产品项目设计、产品原型开发、产品定型和产品验收等阶段,有些仪器要经过临床应用评价等更为复杂的测试过程,涉及力学、电子学、光学、计算机科学、生物化学等学科。检验、检定的过程中,往往涉及到实验科学、工程、检验科学、法律法规等的影响,而营销的过程则受诸多因素的影响。可以说,一种体外诊断设备的成功远不止于设计开发的成功;还需要经得起临床应用和市场检验。
【结论】
2024医疗器械展会Medtec综述了对体外诊断仪器的设计、测试和开发的方法及相关进展进行了系统的概述和总结。体外诊断仪器的开发基于医学检测方法学的发展,同时,体外诊断仪器的设计、测试和开发是复杂系统工程的多学科交叉,需要从力学、电子、光学、检验、计算机科学和控制等多个领域整合工程技术方法,在加工和生产中对材料、工艺和方案有较高的要求。研发过程一般包括产品项目设计、产品原型开发、产品最终确定和产品验收阶段。该综述总结和概述了在这些重要阶段要完成的任务和考虑,此外还分析了体外诊断器械市场的发展趋势,提出了未来产品开发和上市过程中的潜在热点。
文章来源: 抗体故事
















