新型医用涂层如何应用于镁合金血管支架?Medtec中国展分享最新研究进展
2022-07-21
医用亲水涂层产品主要有以下几种应用:导管、支架输送系统、导丝和其他产品。其中,导管占比最大,在2021年,销量市场占比达到了63%。导丝是具有较高附加值的高端医用亲水涂层领域,占比约为20%。目前,发展高端医用亲水涂层是行业的焦点。Medtec中国展也将特邀高效的嘉宾来现场讲解医用功能性涂层在医疗器械中的应用。
采用溶剂热法在镁合金血管支架表面制备了具有微纳米结构的锐钛矿氧化钛涂层,研究了溶剂热反应条件对涂层微观形貌的影响。结果表明,通过改变反应时间,HF含量,及反应溶液中氟离子浓度,可获得不同微纳米结构的氧化钛涂层。随着反应时间延长,锐钛矿晶体形貌由八面体向片层状转变且致密化;随着反应温度升高,片层微结构逐渐增多、片层的厚度逐渐减小;随着溶液中HF含量增加,片状氧化钛的分布逐渐稀疏,涂层化效率降低;随着F-离子浓度增加,片状氧化钛的排列形式趋于分散,由多片交叉叠加向单片演变。反应条件为160℃,10 h , 0.25 mL / HF(40 wt.%), 0.25 mL / NH4F(0.2 M)时,在镁合金血管支架表面制备出了均匀致密,呈片状规整排列的微纳米结构氧化钛涂层,表面粗糙度为350.7 nm。
【研究亮点】
目前报道的镁合金表面氧化钛涂层多为粗糙度极小且微观形貌不可控的涂层,而针对氧化钛涂层微纳米结构设计的研究报道较少。由于细胞在生物材料表面具有特异性吸附行为,若通过特殊工艺制备出具有一定表面粗糙度的微纳米结构氧化钛涂层,将有利于促进血管支架植入人体后的表面内皮化,从而改善支架对病变血管的疗效。基于以上考虑,利用溶剂热反应法在镁合金血管支架上合成了具有特殊微纳米结构的氧化钛涂层,研究了溶剂热反应条件对氧化钛涂层微纳米结构和涂层整体形貌的调控作用。
【研究背景】
钛合金、镁合金等合金因具有良好的力学性能和生物相容性,被越来越多地应用于生物医用材料及器件的研制。而生物医用镁合金材料可在人体内被降解吸收,使得近年来镁合金在可降解心血管支架领域成为研究热点。研究发现,镁合金血管支架目前存在的关键问题是在人体内的降解速率过快,导致支架过早地丧失力学支撑作用。为减缓镁合金血管支架的降解速率,国内外学者开展了大量针对性研究,主要集中在通过表面改性,提高生物医用镁合金的耐蚀性,从而减小其降解速率。如通过各种手段在镁合金表面制备氧化钛、聚乳酸、PLGA、PCL、氟化镁等具有良好生物相容性的防护涂层,较好地改善了镁合金的降解行为。
表面涂层之所以能够有效降低镁合金的降解速率,其根本原因是在镁合金表面形成耐腐蚀层,从而阻断镁基体与腐蚀环境的直接接触。各种涂层材料中,无机涂层是镁合金表面改性选用较多的材料,如TiO2、ZrO2、ZnO等,均能在一定程度上改善镁合金的耐蚀性,减缓镁合金基体的降解速率。其中,氧化钛涂层作为一种无机惰性涂层,可以有效阻止金属离子的释放,起到良好的腐蚀保护作用。除此之外,氧化钛涂层具有优良的抗凝血性,作为镁合金血管支架的表面涂层显示了较好的应用前景。有研究者采用磁控溅射工艺在生物镁合金上制备出氧化钛涂层,证实了该涂层可显著降低镁合金的降解速率。
【研究方法】
镁合金血管支架(合金成分为Mg–2Zn–0.46Y–0.5Nd)在电压为10 V,电流为0.2 A条件下电解抛光5 min,之后在无水乙醇中超声清洗5 min,自然干燥。在容积为28 mL的聚四氟乙烯内胆中加入15 mL无水乙醇作为溶剂,用微量移液器滴入少量质量分数为40%的氢氟酸(HF),然后加入0.5 mL钛酸四丁酯(TBOT)作为溶剂热反应产生二氧化钛的前驱体,将混合溶液磁力搅拌10 min后添加0.25 mL氟化铵水溶液(NH4F),继续磁力搅拌10 min。将准备好的的镁合金血管支架置于反应溶液中,以一定倾斜角度靠于容器内壁。最后将密闭的聚四氟乙烯内胆放入不锈钢反应釜内,在电热鼓风干燥箱内加热至反应温度,反应4 ~10 h,溶液中的前驱体在高温高压下水解生成二氧化钛,并在血管支架的表面形成涂层。将血管支架取出,在去离子水中超声清洗数次,以去除其表面附着的多余反应产物。试验所选取的工艺参数见表1。
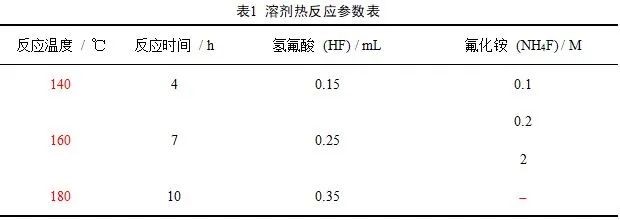
注:NH4F的添加量均为0.25 mL,加入前先配制成不同浓度的水溶液。
采用X射线衍射仪(XRD,PANalytical X’Pert3 Powder,Cu Ka,35 kV,30 mA)分析涂层的物相,衍射角为20~80°,步长为0.01°。采用扫描电镜(SEM,Hitachi SU8000)观察涂层的微观形貌,并配合能谱散射仪(EDS,Cambridge)分析涂层的元素与含量。利用原子力显微镜(AFM,Bruker MultiMode8)分析涂层的微观形貌及表面粗糙度,测试时采用非接触模式。
【研究结果】
溶剂热反应条件160℃, 10 h,0.25 mL / HF(40 wt.%),0.25 mL / NH4F(0.1 M),镁合金支架表面涂层的XRD图谱、微观形貌和原子力表面分析分别见图1~3。从图1可以看出,该条件下涂层的物相为锐钛矿TiO2相。通过溶剂热法在镁合金支架表面制得了致密、均匀的氧化钛涂层,该涂层由约50 nm厚、1 mm宽的层片状结构组成。氧化钛涂层与镁合金基体之间存在较好的结合状况。

图1 涂层材料的XRD图谱
(a) 有涂层的镁合金血管支架
(b) 表面涂层局部放大图
图2 镁合金血管支架表面氧化钛涂层形貌图
原子力显微分析得出该涂层的表面粗糙度为350.7 nm。制备的微纳米结构氧化钛涂层具有宏观平整、微观粗糙的结构特征,这将为深入研究材料表面特征与医用材料生物相容性之间的关系开辟新途径。
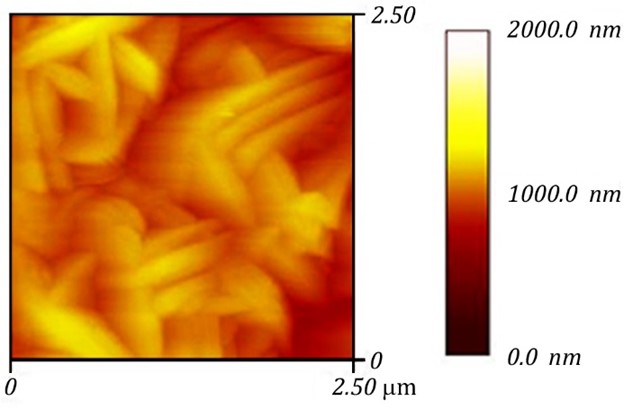
图3 TiO2涂层的AFM表面分析
在160℃, 0.15 mL / HF (40 wt.%) , 0.25 mL / NH4F (0.1 M)条件下,观察氧化钛涂层形貌随时间的变化规律。反应开始阶段并没有形成连续的涂层,镁合金基体大部分处于裸露状态,但已形成了尺度小于1 mm的八面体和片层状锐钛矿晶体,这些晶体以“嵌入”方式与基体结合,说明氧化钛晶体的形核与生长与镁合金基体的晶体结构有直接关系。这种原位生长模式决定了涂层与基体存在较好的结合情况。随着反应时间延长,7 h后涂层变得致密,并出现较多的片状结构,八面体晶体逐渐减少。反应10 h后镁合金表面已经完全被片状氧化钛组成的致密涂层覆盖。
Medtec中国展已经从2012年开始连续举办了7届植入介入医疗器械峰会,会议围绕骨科植入物、心血管介入产品,探讨其法规政策、市场趋势、研发与设计与材料创新等内容,为医疗器械制造商、材料供应商及服务商等提供国内外的经验借鉴。今年作为同期“植入介入医疗器械峰会”的第八个年头,会议内容再次升级,高校、医院、企业的嘉宾讲从材料、临床需求、产品研发等多维度剖析植入介入现状及发展。点击快速预登记。

(a) 4 h (b) 7 h (c) 10 h
图4 氧化钛涂层形貌随反应时间的变化
在0.15 mL / HF (40 wt.%), 0.25 mL / NH4F (0.1 M)条件下,考察了在不同反应温度条件下的氧化钛涂层形貌,见图5。图5a和图5b为140℃和180℃溶剂热反应10 h后涂层的SEM图。同样条件下,结合反应温度为160 ℃时的涂层形貌(见图4c),可以看出,随着反应温度升高,氧化钛片层微结构特征逐渐明显,主要表现为片层结构逐渐增多、片层的厚度逐渐减小。其中,140 ℃时可明显看到片层结构出现,但此时片层结构较为稀疏。当反应体系温度升至160 ℃后,出现了更明显的片层结构特征。180 ℃下涂层由细小、密集分布的微层片构成。这表明反应温度越高,涂层的微结构特征越明显,即氧化钛片层结构的数量越多、厚度越小;同时,锐钛矿晶体分化得越细,形成的涂层整体形貌越致密。
在选用的溶剂热反应体系中,HF的加入量须严格限定在一定范围。图6为溶液中HF加入量对氧化钛形貌的影响。试验发现,当加入较多的氢氟酸(质量分数为40%的HF,0.35 mL),由于前驱体钛酸四丁酯的水解变慢,经过10 h反应后,基体表面形成的氧化钛数量极少,导致涂层极稀疏,氧化钛多以片状晶体形式在基体表面原位生长,见图6a。然而,当反应溶液未添加氢氟酸,则镁合金基体在反应10 h后仍保持其原始表面,没有氧化钛形成,见图6b。这是由于当溶液中的氢氟酸含量较高,导致前驱体的分解速率过快,生成的氧化钛晶核不能与基体充分结合起来。事实上,在不加氢氟酸的条件下,反应1 ~2 h后即有大量的白色沉淀生成,只是这些产物并未与基体结合,而是直接散落在反应容器底部。

(a) 0.1 M

(b) 0.2 M
图7 溶液中F-离子浓度对氧化钛涂层形貌的影响
F-离子浓度对涂层的形貌与微观结构有重要影响,见图7。F-离子的增多导致氧化钛涂层中片状结构排列由密变疏,且由多片向单片逐渐演变。
可以看出,反应时间、反应温度、氢氟酸含量、氟离子浓度等4个参数对氧化钛涂层的微形貌有重要影响。其中,氢氟酸含量的影响作用最大,也是能否形成致密涂层的最关键因素。向15 mL的反应溶液中加入0.25 mL氢氟酸的条件下,得到了理想的氧化钛涂层。然而,增加0.1 mL微量的氢氟酸后(0.35 mL),显著减小了前驱物的水解程度,在基体表面未能形成致密的涂层,从而限制了其实际应用。可见,制备体系需严格控制氢氟酸含量。
研究表明,锐钛矿氧化钛晶体中各晶面的表面自由能不同,(110)、(001)、(010)、(101)等晶面的表面自由能分别为1.09 J / m2、0.90 J / m2、0.53 J / m2和0.44 J / m2。根据Wulff理论,表面自由能较高的晶面,在晶体自然生长中不会被暴露;而表面自由能较低的晶面,最终会暴露出来。故锐钛矿晶体的暴露面一般为表面自由能较低的(101)晶面。本课题的氧化钛晶体中(101)晶面所占的比例很小,片状微纳米结构是氧化钛晶体在发育过程中沿着和晶向优先生长所得到的,这种晶体生长模式与F-离子的作用存在密切关系。在锐钛矿晶体最初生长过程中,如果有一定数量的F-离子吸附在(001)晶面上,就会大大限制氧化钛晶体沿c轴即方向的生长。YANG H G等基于第一性原理,对各种离子吸附情况下锐钛矿(001)和(101)晶面表面能进行了计算,结果表明吸附F-离子后,(001)面表面能显著低于吸附F-离子的(101)表面自由能,这种情况下(101)面的生长受到限制,从而使晶体发育完成后最终的暴露面为(001)面,故F-离子的存在使得所获得的涂层是由(001)面外露的锐钛矿晶体构成。图8为160℃,10 h,0.25 mL / HF(40 wt.%) , 0.25 mL / NH4F(0.2 M)条件下,氧化钛涂层表面EDS能谱图,F元素的存在证实了氧化钛涂层形成过程中F-离子的吸附作用。
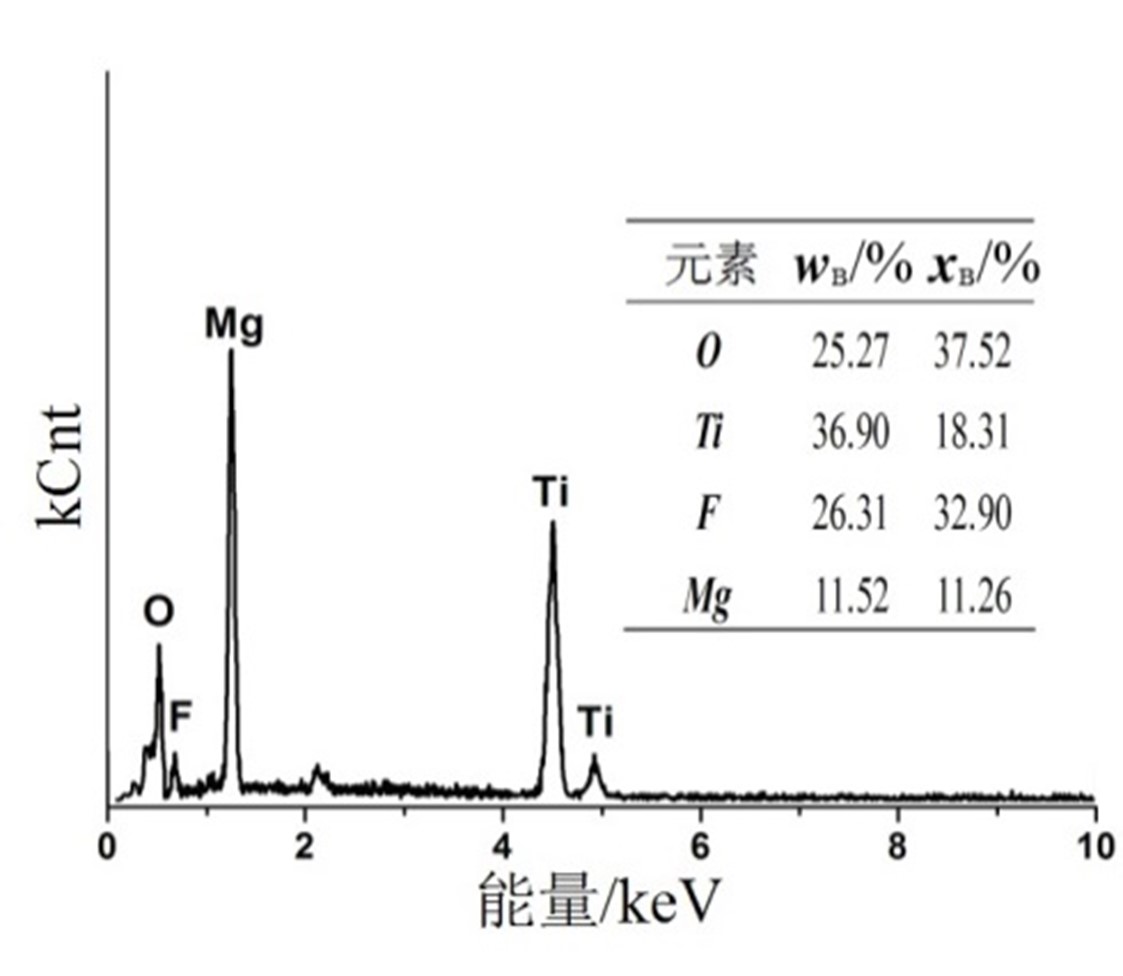
图8 氧化钛涂层的能谱分析
【Medtec中国展分享结论】
(1) 针对生物医用镁合金面临的问题,选用无水乙醇作溶剂,在较低的反应温度下,通过溶剂热法在镁合金血管支架表面合成了锐钛矿氧化钛微纳米结构涂层。
(2) 通过改变溶剂热反应条件,可实现镁合金血管支架表面氧化钛涂层的微观形貌调控。反应时间、反应温度、氢氟酸含量及F-离子浓度的变化直接影响了涂层的致密度、表面粗糙度及微纳米结构的排列。
(3) 反应条件为160℃,10 h , 0.25 mL / HF(40 wt.%), 0.25 mL / NH4F(0.2 M)时,可获得均匀致密,呈片状规整排列的微纳米结构氧化钛涂层,表面粗糙度为350.7 nm。
侯树森,李悦,杨婷婷,等.镁合金血管支架TiO2涂层的微形貌调控[J].特种铸造及有色合金,2022,42(4):472-476. HOU SS,LI Y, YANG Z J , et al. Micromorphology control of TiO2 coating prepared on Mg alloy stent[J].Special Casting & Nonferrous Alloys,2022,42(4):472-476.
来源:特种铸造












