通过率不到10%,5大领域占比近七成,FDA“突破性设备”有什么启示?医疗自动化制造设备展市场观察
2023-03-07
近年来,在政策助力和资本扶持下,我国医疗器械行业整体水平不断提升,2022年我国医疗器械市场规模预计达9,582亿元人民币,近7年复合增速约17.5%,已跃升成为除美国外的全球第二大市场。从国内医疗器械行业从从一穷二白到各领域全面开花,并逐步突破核心领域及关键技术,甚至在某些领域达到了国际先进水平。与高速发展相对的是我国在高端医疗器械的创新上距离全球先进水平仍有相当差距。看清差距,或许更有利于今后的对症下药。
近日,医疗自动化制造设备展Medtec China 2023了解到,FDA和NMPA先后发布了2022年医疗器械创新方面的总结。希望能够厘清我国与全球先进水平在医疗器械创新方向上的不同,以为行业参考。
累积纳入760款仅62款获准上市,FDA“突破性设备”宽进严出
历经多年发展,美国在医疗器械创新上的地位无可撼动。一方面,美国拥有全球绝大多数顶尖医疗器械公司,在研发上有海量投入;另一方面,通过一系列顶层建设,美国扫清了高校创新的障碍,使其能力得到极大释放。
除此以外,监管机构也尤为重视鼓励创新。作为医疗器械上市的审批单位,FDA从2018年开始设立了“突破性设备”计划,用以鼓励创新医疗器械的发展。其范围涵盖了上市前批准申请(PMA),上市前通知(510(k))或De Novo分类申请框架下进行审核。
简单而言,PMA风险等级大体与国内3类证相当,通常需要完成临床试验与实验室测试。510(k)风险等级则与2类证相当,其基本过程是通过提交与市面已获批医疗器械的对比,证明申请器械实质性等同参照器械即可。
所谓实质性等同指申请器械至少与已上市产品同样安全或更安全,且不能引起有关安全及有效性的任何问题。因此,这一流程可以大幅提升获批效率。
若中低风险医疗器械没有找到可参照的实质性等同器械,则可以申请进入De Novo通道。一旦进入De Novo通道,则后续可以进一步提交510(k)申请,类似于我国的2类创新医疗器械。
“突破性设备”可以明显缩短这些医疗器械的获批上市时间,因此它取代了之前的快速访问途径(EAP——Expedited Access Pathway)和优先审查(PR——Priority Review)。
要想进入“突破性设备”清单,则需要满足下列标准。
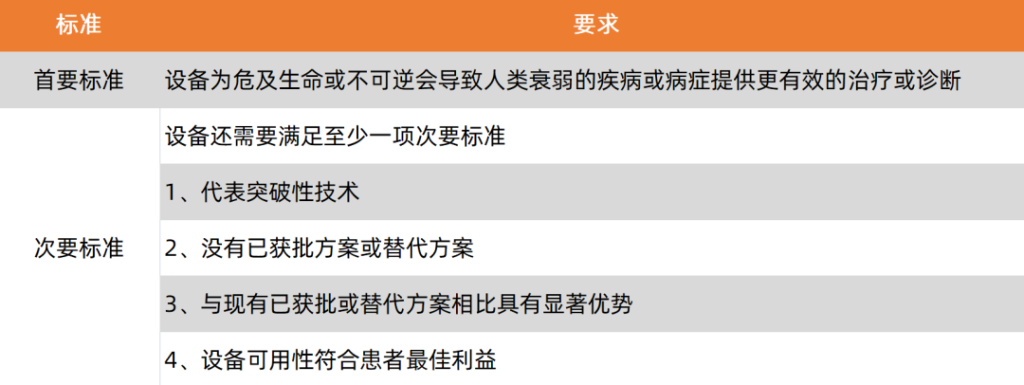
基于美国医疗器械在全球的领先地位,FDA的“突破性设备”事实上代表了全球医疗器械创新的顶尖水平。
除了“突破性设备”,FDA还在2021年设立了“医疗器械安全技术计划”(STeP——Safe Technology Program),用于覆盖不符合突破性器械计划的医疗器械。这些器械虽然有其创新之处,但所针对的疾病往往并不严重,达不到“突破性设备”的紧迫程度。
从2015年开始截至2022年12月31日(之前通过EAP计划纳入的器械也被FDA计算在内),共计有760款医疗器械被纳入“突破性设备”名单。这其中,除了8款由主管生物制品的CBER(生物制品评价与研究中心)通过,其余752款均由主管医疗器械和数字医疗的CDRH通过申请。
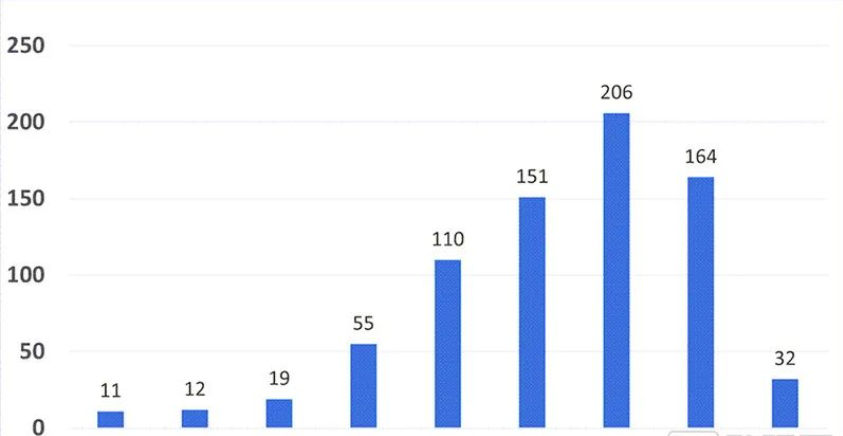
历年FDA“突破性设备”分布(本图为按FDA财年划分,对应截至自然年时间为2022年12月31日,图片来自FDA官网)
如果按领域划分,“突破性设备”共可被分为20个领域。这其中,针对心血管的“突破性设备”数量最多,历年共有171款。其次则是针对神经领域的“突破性设备”,共有137款。在这之后则是骨科(87)、肠胃科(60)和整形外科(53)。
医械市场日新月异,如何精准快速把握市场变局与转变方向?来医疗自动化制造设备展Medtec China 2023第七届医疗器械市场分析报告论坛,今年6月3日在苏州国际博览中心举办,盘点当下医疗器械/医疗行业最新发展趋势和热点与介入器械:带量采购常态化背景下的投资现状与趋势。来自中国医疗器械行业协会、弗若斯特沙利文咨询、苏州益道等机构和企业均来到现场分享市场情报的观点。点击快速预登记。
这5个领域的“突破性设备”累计数量达到了508款,占比高达66.8%。这也代表了目前全球顶尖医疗器械创新主要的方向和趋势。
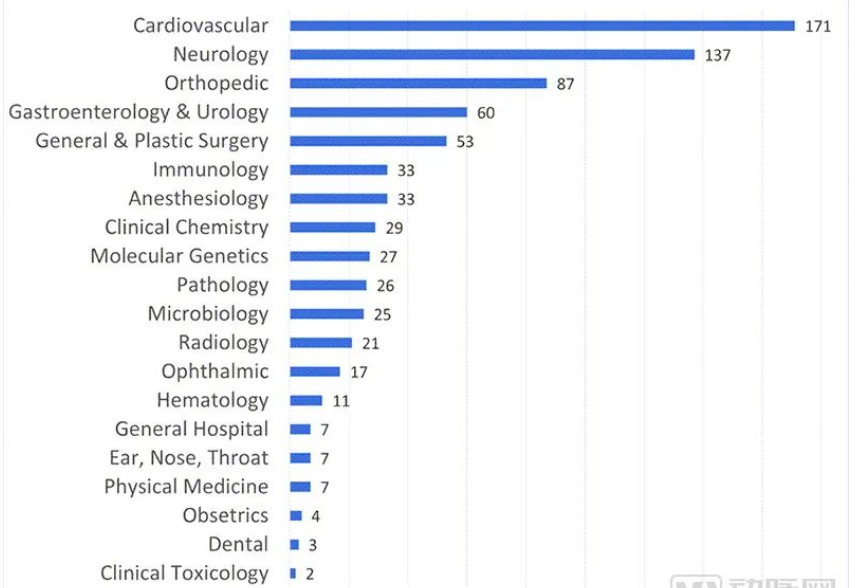
FDA“突破性设备”数量分布(按领域划分,截至2022年12月31日,图片来自FDA官网)
不过,虽然入选名单看似庞大,但真正能够获准上市的其实并不多。从2015年至今,一共也仅有62款“突破性设备”获得了FDA的上市批准,通过率其实仅有8.9%而已。
2022年,一共有19款“突破性设备”最终获准上市。这其中,也包括了首个用于阿尔茨海默症早诊的IVD设备、首次运用眼动追踪技术评估儿童ASD的设备以及全球唯一可用于DCD心脏移植的系统。
● 首个用于阿尔茨海默症早诊的IVD设备
富士瑞必欧的Lumipulse G ß-amyloid ratio是首个用于早期检测与阿尔茨海默症相关淀粉样斑块的体外诊断测试设备,可用于评估55岁及以上认知障碍患者认知能力下降的原因是否与阿尔茨海默症相关。
Lumipulse测试则通过测量人脑脊液(CSF)中发现的β-淀粉样蛋白1-42和β-淀粉样蛋白1-40(可以积聚并形成斑块的特定蛋白质)浓度的比例,并与其他临床评估结合使用帮助医生初步筛查患者脑部是否可能存在淀粉样斑块,进而再决定下一步诊断和治疗。
在这一创新医疗器械获准上市之前,医生只能使用影像设备来检测认知障碍患者大脑中的淀粉样斑块。对于患者来说,影像扫描耗费时间且价格昂贵,也存在辐射风险。Lumipulse G ß-amyloid ratio仅需一天就可完成测试并出具报告,价格相对便宜,且没有潜在的辐射风险,可为阿尔茨海默症的早期诊断提供很好的选择。
● 首次运用眼动追踪技术评估儿童ASD
Earlitec Diagnostics的Earlipoint System创新性地采用了眼动追踪技术,可用于16-30个月儿童的ASD(孤独症谱系障碍)评估。
该系统利用社会-视觉参与动态量化(DQSVE)可以捕捉儿童在观看一系列描述儿童社交互动短视频场景时难以被人眼察觉的细微行为来对儿童注意力和响应能力进行评估。评估由训练有素的技术人员进行,应用场景为一名儿童观看一系列描述儿童之间社交互动的短视频。
眼动追踪技术以每秒120次的速度评估各个焦点,然后将每个数据点与临床验证数据库中的数千个离散测量值进行比较,利用专利分析技术将结果与预期年龄参考指标对比,并提供与社会残疾水平以及语言和非语言能力相关的EarliPoint严重性指数,进而实现ASD患儿的早期识别。
医疗自动化制造设备展Medtec China 2023同期现场会议第七届医疗器械市场分析报告,议题覆盖医疗器械/医疗行业最新发展趋势和热点、带量采购背景下医疗高值耗材的成本品质控制、介入器械:带量采购常态化背景下的投资现状与趋势等
● 全球唯一可用于DCD心脏移植的系统
TransMedics自主研发的便携式器官保存系统Organ Care System (OCS) Heart System是首个能将自然死亡后捐赠的心脏保存在温暖的跳动状态下的装置,也是FDA唯一批准的用于保存标准和扩大标准供体心脏的设备,还是全球唯一可用于DCD心脏移植的系统。
器官移植的时效性极为重要,如心脏仅能承受8小时的冷缺血时间。若器官长期处于冷缺血状态,将会导致永久性损伤。临床上通常采用“静态冷藏法”来保存器官。即从人体摘取器官后先向器官内注入保存液,而后将器官放入冷藏箱内,利用低温来减缓器官的新陈代谢过程。
但这种方式已经逐渐暴露出一些问题,如器官长时间冷藏后功能受损,且医生无法监测器官功能状态等。因此,利用机械灌注在体外为器官复制一个体内环境,从而保持器官的正常代谢是器官保存技术的新方向。
Organ Care System (OCS) Heart System通过向器官灌注温暖、含氧、营养丰富的血液,模拟人体新陈代谢的状态,以减少器官缺血时间,维持器官活性。医生还可以通过该系统实时监测器官的功能与活性,评估其是否可用于移植。
全年纳入68款获批55款,我国创新医疗器械审批创历史新高
无独有偶,NMPA也在近期发布了我国2022年医疗器械总结,并对创新医疗器械注册审批进行了回顾。
2022年,共有343款医疗器械申请创新医疗器械特别审批,比2021年增加37.8%。其中68款获准进入创新医疗器械特别审查程序,比上一年略多。通过创新医疗器械通道获批55款,比上一年大幅增加57.1%。
从2014年至2022年,NMPA共批准189个3类创新医疗器械。其中,境内创新医疗器械涉及15个省的134家企业,进口创新医疗器械涉及2个国家的8个企业。
2019年是我国创新医疗器械新规开始实施的第一年,从彼时起,我国医疗器械创新开始逐步成长,无论是申请数量、进入程序数量和最终获批的数量都在逐年增加。2022年,各项指标都创下了历史新高,甚至超越了新规实施前巅峰的2017年(进入程序)和2018年(申请数量)。从数量上来看,医疗器械行业的创新热情的确得到了激发。
事实上,这仅是国家局对3类创新医疗器械的统计。如果加上由地方局审批的2类创新医疗器械,数量将会更加庞大。根据动脉网的不完全统计,2022年各地方局纳入创新医疗程序的2类医疗器械至少为89款。
需要指出的是,各地对创新医疗器械的审批不完全相同。比如,有的地区特别设置了2类创新医疗器械审批程序,有的地区则是在优先审批医疗器械中包含了创新医疗器械。
单纯从数量上而言,我国医疗器械创新的确呈现出朝气蓬勃的景象。不过,由于我国医疗器械行业尚需进一步发展,相当数量的“国内首创”创新医疗器械仍处于填补国内空白的阶段,能够达到“各项性能指标达到国际同品种器械水平”评价的器械也并不算多。总体而言,我国医疗器械距离全球先进水平仍有一定差距也是客观事实。
不过,2022年,仍有几款值得一提的获批创新医疗器械,在技术水平和设计上达到了行业领先水平,并在NMPA给出的评价中予以体现。
● 全球独一,首个通过体内振动改善功能性便秘的胶囊机器人
这一产品由上海安翰医疗技术有限公司推出,于2018年申请成功纳入创新医疗器械审批流程,并于2022年2月最终获批,被NMPA认为是“同类首个,目前国内外尚无同类产品上市”。
目前,便秘治疗虽然有多种方法可供选择,但存在患病率高、治疗副作用大、复发率高和病人满意度低的情况。这种一次性使用的消化道振动胶囊可通过振动对结肠壁进行刺激,促进结肠蠕动,为药物治疗效果欠佳的成人功能性慢性传输型便秘提供非药物治疗的全新治疗办法。
● 全球首款双源、双探测器口腔CBCT
北京朗视仪器股份有限公司的这款创新医疗器械于2020年纳入创新医疗器械审批程序,并于2022年7月获批,“是全球首款双源、双探测器的口腔CBCT产品”(NMPA评价)。其核心技术为双源成像技术,通过小焦点、高功率X射线管头和高分辨率探测器提升空间分辨率,在满足口腔颌面部成像需求的基础上,为耳鼻喉科疾病提供X射线锥形束体层摄影检查。
它具备大、小两种视野成像系统,大视野成像系统可用于口腔颌面部、鼻部和咽喉部气道的常规成像检查,小视野成像系统则具有高空间分辨率,用于耳部内部机构(中耳、内耳)的成像检查。
在此之前,医院主要采用通用CT进行耳部影像检查,存在分辨率不足、关键结构无法显示、隐匿病变难以看清等不足。这一创新医疗器械的推出能够有效解决通用CT对耳科精细解剖结构成像不清的难题,从而推动耳科疾病的基础研究和临床诊疗。
● 火速获批的5.0T全身磁共振系统国际领先
该器械由上海联影医疗科技股份有限公司推出,于2022年初获批进入创新医疗器械程序,核心技术“拥有自主知识产权,关键性能指标已达到国际领先水平”(NMPA评价),并于2022年8月火速获批,整个审批流程不足一年,在创新医疗器械中实属罕见。
基于3.0T的时间飞跃磁共振血管成像能够清晰显示脑血管结构,是目前临床一线的无创脑血管成像技术。但其抑制背景组织信号不佳,对大血管远端分支和细小穿支动脉的评估无法满足临床需求。超高场强7.0T技术可以解决这一短板,但场强的提升会使得B1场的不均一性和受试者生理不适感增加。
5.0T磁共振系统则实现了平衡,首次突破了超高场磁共振局限于脑部成像的限制,可实现超高场全身临床成像;在神经系统成像方面更是比肩更高场设备,可为脑小血管疾病与退行性病变提供更多诊断信息。
对比先进水平,我国医疗器械创新发展空间巨大
从两国创新医疗器械审批不难看出,我国医疗器械创新较全球先进水平仍有提高空间,但近年来发展势头迅猛也是不争的事实。
对比FDA的突破性设备和NMPA的创新医疗器械审批,FDA的风格更偏向于“宽进严出”。尽管历年纳入名单的器械数量十分庞大,但最终拿到上市申请的占比仅有8.9%。
相比之下,我国创新医疗器械审批则有所不同。根据历年情况汇总统计,在获准进入创新医疗器械程序这一步的通过比例约为21%,但在进入创新医疗器械审批程序后成功拿到医疗器械证的比例则高达51%。如果再加上各地方局的2类创新医疗器械,通过率或许会更高。
不过,考虑到我国创新医疗器械目前还处于国产替代、微创新和跟随式创新阶段,这种情况也实属正常。
值得一提的是,我国创新医疗器械的同质化程度明显较高。以2022年进入创新医疗器械通道的产品为例,心血管类创新医疗器械为第一大类,占比超过一半。相比之下,心血管类器械虽然也是“突破性设备”第一大类,但所占比例远不一样。
此外,在2022年,手术机器人进入创新医疗器械名单的数量仅次于心血管,但这些产品是否都能够满足临床需求,或许也需要进一步观察。
这一现象的背后,也折射出我国医疗器械创新与全球顶尖水平的差距,包括在研发的投入、科研转化、基础科学的加强乃至后续的进一步产品化和商业化上。我国医疗器械创新仍然有相当长的路要走。
好消息是,基于巨大的需求,国家对医疗器械创新愈发重视,医疗新基建浪潮持续落地对于国产龙头企业也是巨大利好。同时,政策有意扶持,国产替代和医保支付对创新医疗技术都给予了一定的优惠,使得创新成果有机会在更短时间实现商业价值,从而快速成长。此外,背靠我国强大制造业基础,医疗器械创新也有较好的发展基础。
我们相信,国内医疗器械创新在未来必然会呈现更好的发展,也终将会在全球版图中占据重要的地位。
文章来源:动脉网












