“科学的选择验证规格,是做好性能验证的第一步”。
2025上海医疗器械创新展Medtec解读医疗器械的设计性能验证,需要考虑两个基本问题:1、选择哪些规格进行验证才最具有代表性?2、选择什么样本量才能够达到验证目的?本文根据ASTM F3172的方法,以血管内器械为例,解读设计验证样本规格和样本量选择。
一、规格型号选择的影响因素
型号规格的选择主要考虑以下几方面因素:
a) 设计输入的性能要求(Design Input Requirement)对应的基本设计输出;也就是产品的设计参数(尺寸、材料等)。
b) 设计子组;对所考察的性能不产生影响的设计输出参数组合。
以血管内球囊导管为例,如下图所示,该产品按球囊尺寸划分,包含10-50mm长度尺寸和3-7mm直径尺寸共25个规格。
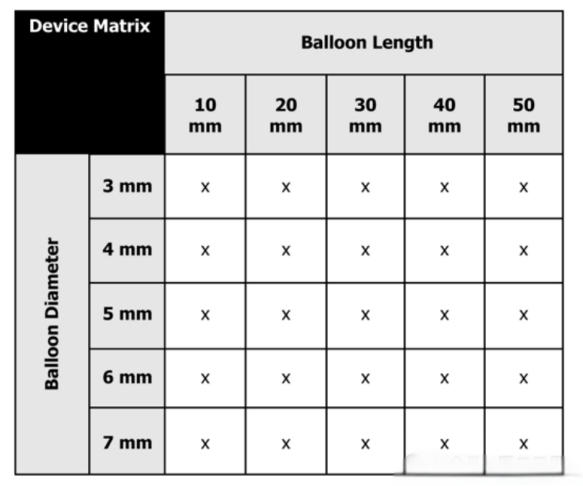
我们列出几个需考察的性能,以及其对应的基本设计输出(EDOs):
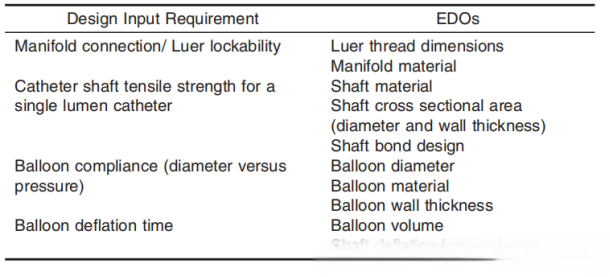
(1)鲁尔接头锁定性
分析鲁尔接头的锁定性的影响因素,得出其基本设计输出的要求为:鲁尔连接螺纹结构尺寸和材料的选择。
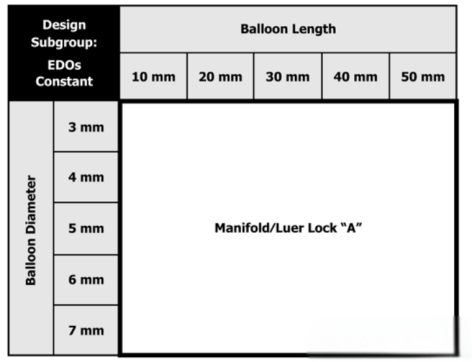
我们可以知道,对于产品规格矩阵中的球囊长度和直径参数,其变化并不会影响到鲁尔接头的性能,因此所有的规格都在一个设计子组中。或者说,我们在这个规格矩阵中,任意选取一个规格都能够代表产品的鲁尔接头锁定性能。
(2)导管的抗拉性能
导管抗拉性能的基本设计输出为:导管管体的材料、截面尺寸(直径和厚度)以及粘接段的设计等。由于这些设计参数的存在差异,所以将相同设计的规格归为一个设计子组,就产生如下的矩阵分组。2025上海医疗器械创新展Medtec指出如表中所示,设计A和设计B存在差异,如果我们仅在A设计中选择一个规格进行验证,就不能够覆盖B组中的性能。因此,我们在选择验证规格的时候,就要考虑从A组和B组中,各选取一个规格进行验证。
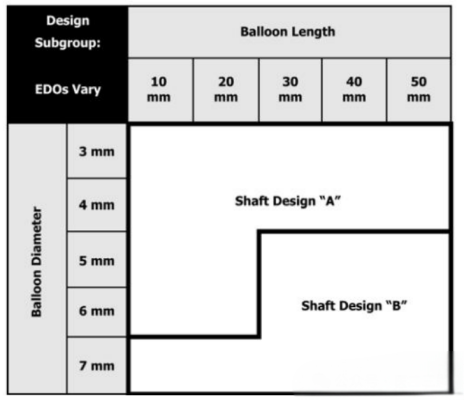
(3)球囊顺应性
球囊在给定的压力下,达到设定的直径尺寸。影响因素主要有:球囊直径、球囊材料和球囊壁厚。以此区分出不同直径的球囊为一个子组,组内的设计输出是一致的。

二、规格选择方法
当我们分析了性能影响因素和规格之间的差异后,我们有以下方法进行设计性能验证的尺寸选择。
1.在每个设计子组中,选定一个规格进行测试。
比如对球囊导管的拉断力测试,就要从设计A和设计B中分别选择一个或多个规格进行测试,以充分验证产品拉断力满足要求。
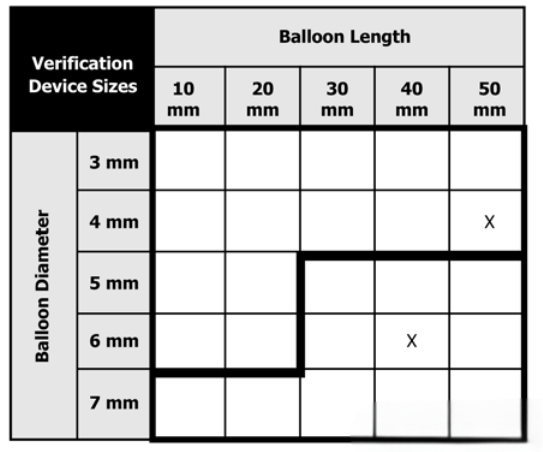
2.选择最差工况下的设计子组,进行测试。
2025上海医疗器械创新展Medtec现场将设四大专区,囊括电子光学、AI、IVD诊断及影像、检测、临床、法规、研发设计& 大动物实验专区等展品,点击此处报名参展>>>
最差工况(worst case)是进行性能验证的常用方法。
(1)通过结构分析、历史经验等方式,选择最具挑战性的规格,就能够反映所有的规格的符合性情况。比如强度通常与尺寸相关,洁净度通常与面积相关,显影性通常与材料分子量相关。
例如:我们在考察球囊导管管体的拉断力时,当我们明确知道设计A的界面尺寸较小,相比较来说,是薄弱的,理论分析后,明显小于设计B的拉断力,那么在同样的应用状态下,设计A就是worst case。
(2)通过模拟计算(有限元等)
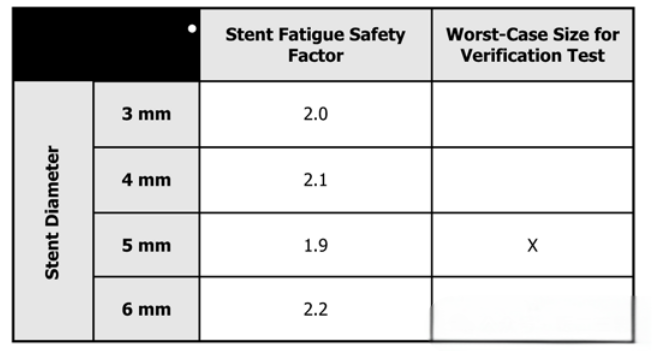
但有些时候,我们并不能够简单地通过分析得到最差工况的规格。比如在确定支架疲劳性能的最差工况时,可对每个直径或其他相关特性(例如设计平台、长度)规格进行有限元分析,以确定疲劳安全系数以及临界应力和应变值和位置。将预测的应力和应变与疲劳寿命线进行比较,以确定疲劳安全系数。2025上海医疗器械创新展Medtec认为疲劳安全系数最低的植入物可以作为设计验证中最坏的情况进行测试。
3 测试设计子组中一个子集(即多个规格)
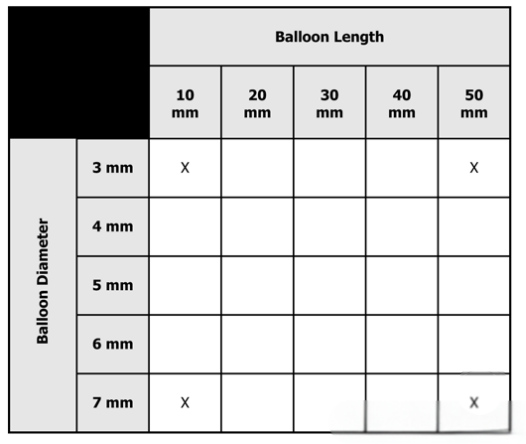
有些设计特征,在所有的规格中都是变化的,当我们无法确定最差工况的规格时,就需要增加规格数量,如下图,可采用四角法,对边缘规格、极限尺寸分别进行测试。
结语
从风险的角度来分析,设计性能验证的规格选取,就是要找到性能最薄弱的环节,因此,要全面评估每个性能的影响因素,然后通过经验、理论计算、模拟计算等手段,确定worst case。当无法确定worst case时,就要增加规格的覆盖范围,优先选择边缘规格、四角规格等,以保证验证的全面性。